1、 首先是能量最低原理,电子倾向于先占有能量最低的轨道,我们知道原子核外电子排布的轨道依次是:s 、p、d、f、...这样的顺序排列的,其中s轨道能量最低,这就使电子最优先在s轨道上排列。

2、 其次是洪德规则,能量相等的轨道上若自旋平行的电子数最多时整个体系的能量最低。即在能量最低原理的基础上,如果在一个能量相同的轨道上,例如p轨道上,有三个电子,则这三个电子相互平行排列的时候能量使最低的。

3、 最后是每个轨道上最多容纳一个自旋平行的电子;这个要求就是说在一个相同的轨道上只能容纳一个状态的电子。例如s轨道,如果有两个电子,则他们是反平行排列的。

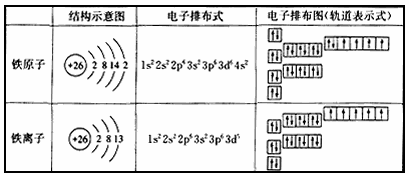
1、 综合以上可得,满足上面几个条件的时候,原子是出于基态的;原子在得到或则失去电子的过程中,也是按照这些规定的。例如三价Fe离子,由于Fe的外层电子分布式是3d64s2,失去三个电子,形成电子分布变为3d5。所以最后形成所以是9~17电子构型。